GMP法规,GMP合规,GMP认证,GMP咨询,制药合规,制药行业,药品监管,质量管理,德恩咨询,gempex,清洁验证,除菌过滤,PUPSIT
在无菌药品生产领域,中国 GMP 明确要求除菌过滤器使用后进行完整性测试。但随着行业质控要求不断提升,当前行业实践与监管关注的焦点,已日益转向一项并未被法规明文强制、却广受认可的操作 ——PUPSIT(使用前灭菌后完整性测试)。
不少同行在面临一个现实困境:法规没要求PUPSIT,我到底要不要做?如果不做,如何应对检查呢?
困境的核心:字面合规VS实质风险

单纯从现行中国GMP无菌附录的条文本身来看,仅执行“使用后”完整性测试,是满足法规的强制性要求的。然而,现代GMP合规的内涵不止于对条文的字面遵守。检查官关注的,不仅是有没有违反某条具体规定,更是整体控制策略是否科学、充分,能否确保无菌保障万无一失。
只做“使用后”完整性测试,就像在菜肴出锅后才检查锅是否漏了,一旦失败,整批产品将面临报废风险。而PUPSIT,则是“在下锅前给锅做一次安全检查”,将风险拦截在发生之前。
国际视野:PUPSIT已是明确方向

PUPSIT并非凭空而来,它源于国际主流监管机构的要求。目前,国际主流监管机构正在将风险前移的理念写入法规。
这一国际趋势也影响着国内的法规修订进程。2025年发布的中国GMP无菌附录征求意见稿中,第187条也已计划将PUPSIT纳入未来的法规要求。

因此,检查官对PUPSIT的关注,是基于前瞻性的风险管理视角,在某种程度上也反映了国内监管与国际标准和理念接轨的趋势。
现实的选择:做还是不做?
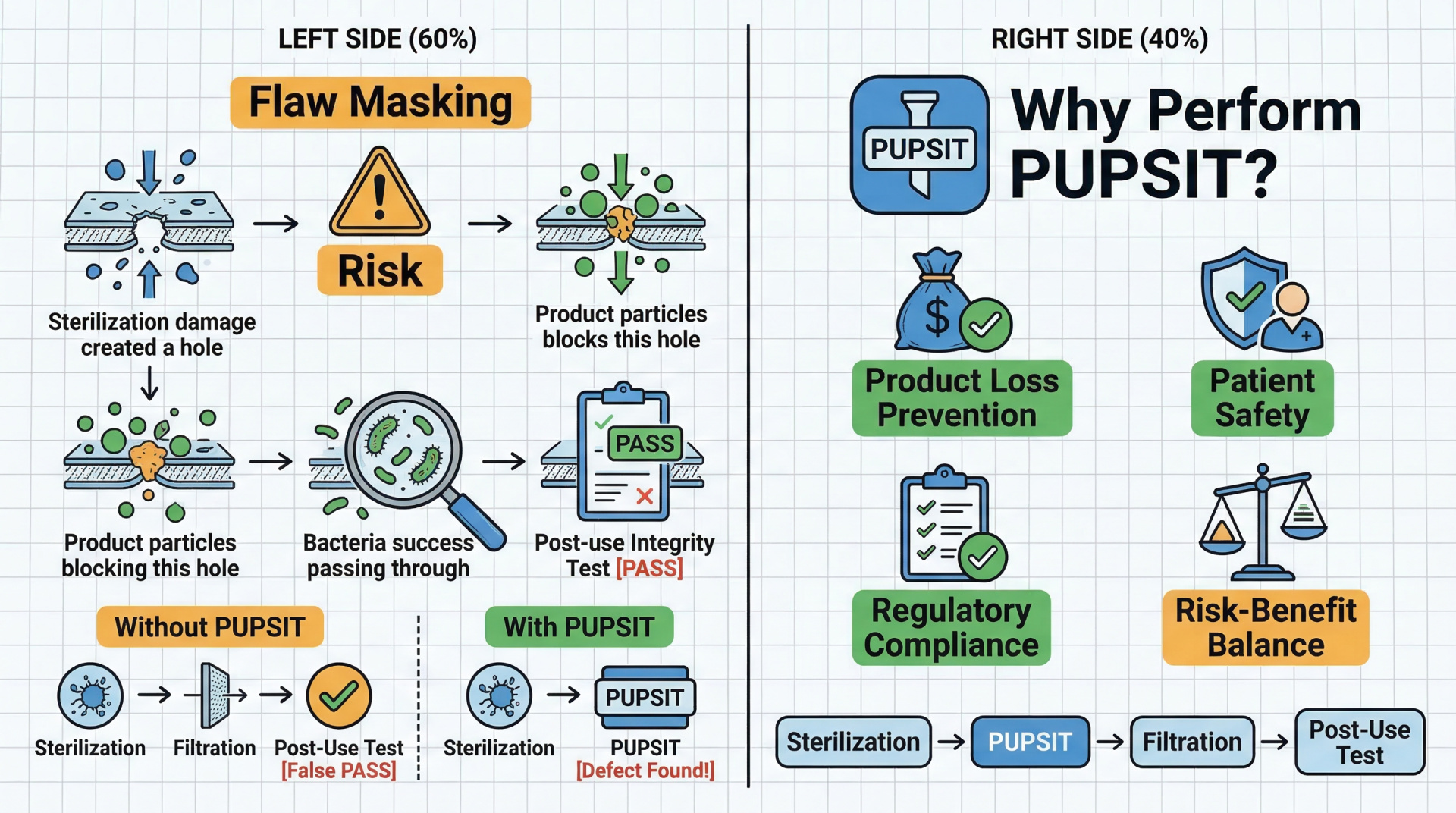
选择做PUPSIT:
选择不做PUPSIT:
需要注意的是:若产品目标市场为欧盟地区,欧盟已对 PUPSIT 实施强制性法规要求;仅在特殊情形下,方可豁免该项测试,通过其他针对性控制措施实现风险管控。
关键行动:如何证明选择合理?
如果决定执行PUPSIT,需要准备至少以下文件:
1. 验证文件 : 将PUPSIT纳入培养基模拟灌装(APS)验证中。
2. 详细SOP :涵盖测试操作、失败调查、滤芯更换、产品追溯等完整流程。
3. 完整批记录 :测试结果、操作人、时间以及失败时的调查记录、纠正预防措施记录。
在工艺限制的情况下决定不做PUPSIT,需要准备:
1. 全面的工艺验证数据 :证明灭菌工艺、安装操作极其稳健,历史数据表明在“使用前”失效的概率极低。
2. 强化进料控制证据 :例如,对每支进厂的除菌滤芯进行100%的完整性测试
3. 综合风险评估报告 :用数据量化论证,证明整体风险水平不高于执行PUPSIT。
结语
在无菌药品生产领域,合规的门槛正在不断提高。PUPSIT的现实困境,本质上是企业从“被动合规”迈向“主动质量保证”过程中必须作答的考卷。它考验的不仅是技术能力,更是企业基于科学和数据决策、并能用完整证据链清晰阐述其逻辑的体系成熟度。
为了帮助您快速评估企业除菌过滤系统完整性测试的实施现状,我们整理了一份除菌过滤器合规自查清单(点击下载)。您可以根据实际情况逐项核对。
关于我们
gempex德恩咨询作为源自德国的GMP咨询与执行机构,深耕合规领域20余年,专注将复杂法规要求转化为可落地的企业实践。我们的专家团队在工艺验证领域拥有丰富的经验,尤其是无菌工艺验证、清洁验证等方面具备实战经验。我们可为您提供以下支持:
如果您需要第三方专业视角进行审计,或者需要能够落地的合规解决方案,欢迎联系我们。
点击下方图片,了解我们完整的合规服务类型。 让我们用专业的合规能力,为您的产品质量保驾护航。
如果您想了解更多GMP解决方案,可以访问www.gempexchina.com/gmp-knowledge获取。在那里,您将更深入了解gempex德恩咨询的GMP服务。
如果您有具体的合规难题,请通过以下方式联系我们。
热线:400 166 2002
邮箱:info-cn@gempex.com
关于gempex德恩咨询
gempex德恩咨询深耕GMP合规领域24年,致力于为全球的生命科学企业提供合规、高效及可执行的GMP解决方案,帮助制药、生物技术、原辅包、医疗器械等各方达到NMPA、EU、FDA、PIC/S等GMP标准,减少合规及药品安全风险。
目前,我们拥有60多位经验丰富的GMP专家,全球累计执行项目超过5000个,累计为1000多个客户提供专业服务,业务遍布20多个国家,并与众多知名药企建立了长期的合作关系。