WLQCL,GMP合规,WHO,药品出海,制药行业,药品检测,德恩咨询,gempex

如果你的药品计划拓展海外市场——无论是出口到非洲、东南亚、南美等地区,还是申报WHO药品预认证(PQ)、参与联合国采购及其相关国际组织的集中采购,那么您大概率会遇到一个关键问题:
国际组织和海外监管机构,是否认可您所选择的委外检验实验室?
换句话说,您提交的第三方检测报告,是否具备通行全球的技术信誉?这很大程度取决于该实验室是否已被列入 “世界卫生组织列名质量控制实验室(WLQCL)” 名单。
这正是今天要深入探讨的主题,我们将用一篇文章为您讲清楚:WLQCL到底是什么?它对药企有什么用?
WLQCL是什么?
WLQCL是WHO认可的实验室名单。列入名单的实验室,意味着:
药企为什么要关注WLQCL?
很多人以为WLQCL只是“实验室”的事,和药企无关。实际上,无论是药品检测数据的使用方,还是有意提升内部实验室资质的药企,WLQCL都值得关注。具体价值如下:
|
价值类型 |
具体好处 |
|
商业机会 |
|
|
技术提升 |
|
|
声誉增强 |
通过WHO严格评估,本身就是实验室水平的权威证明。国内外监管机构对此类实验室出具的数据信任度更高,企业在国际合作中的专业形象也随之提升。 |
需要说明的是:生产端GMP合规(如FDA 21CFR、EU GMP)是药品出口的基本门槛,WLQCL是在此基础上的进阶资质。二者属于不同维度的认可,互不替代。
如何申请WLQCL?
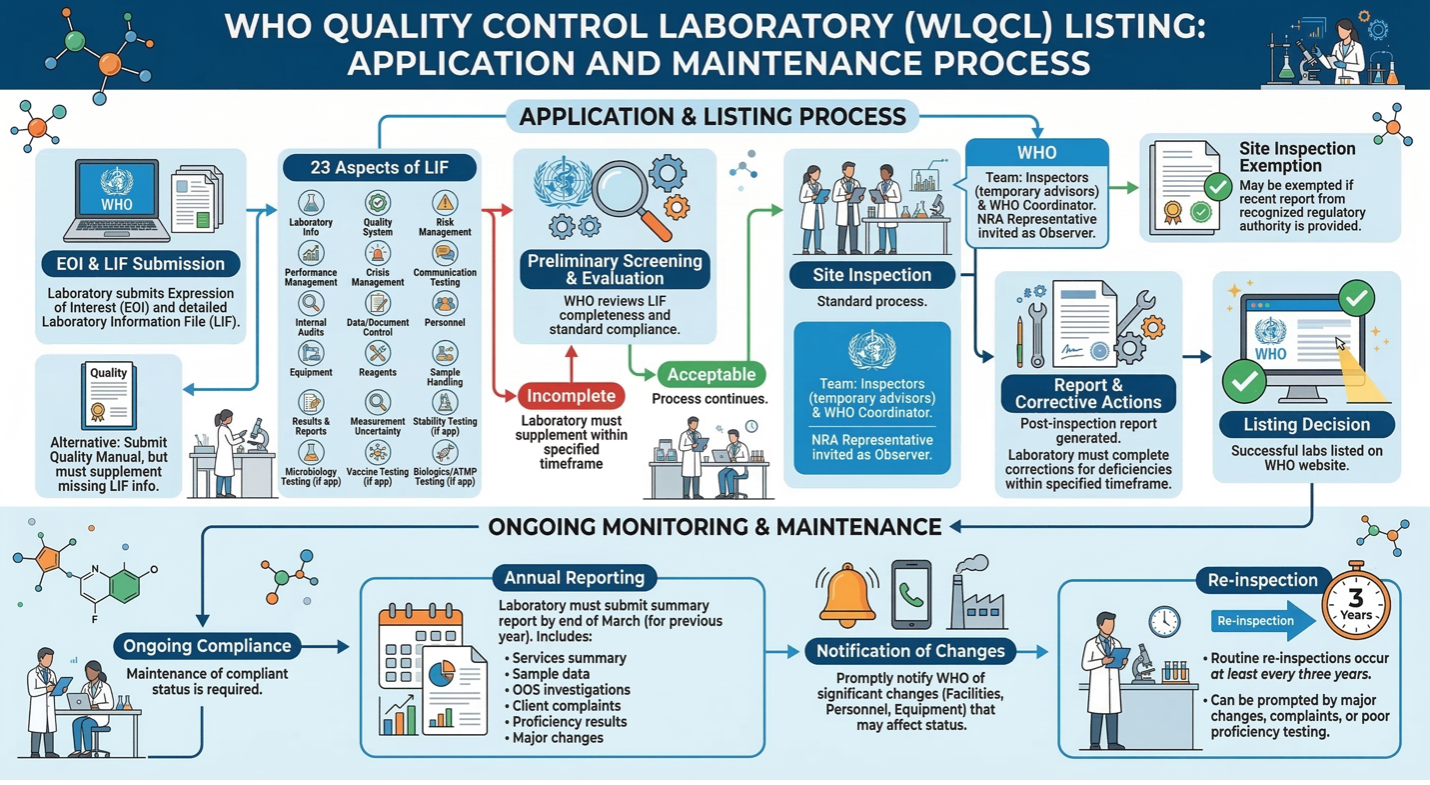
1、获取邀请与参与
2、意向表达
LIF是申请的关键材料,其编制应该遵循《实验室信息文件编制指南》(Guidelines for preparing a laboratory information file),具体涵盖 23 个方面,包括:
1) 实验室一般信息:包括实验室概况及拟申请列名的检测活动范围。
2) 质量管理体系:已实施的质量管理体系,以及实验室曾接受的检查和外部审计。
3) 风险管理
4) 绩效管理
5) 危机管理
6) 沟通管理
7) 能力验证参与情况:参加能力验证计划和/或协作试验的记录。
8) 内部审计
9) 数据、文件和记录控制
10) 人员
11) 设施与场所
12) 设备
13) 试剂、参考物质及标准材料
14) 检测分包(如涉及)
15) 样品处理
16) 分析程序的验证与确认
17) 结果评估与报告
18) 结果超标(OOS)调查
19) 测量不确定度
20) 稳定性测试(如涉及)
21) 微生物检测(如涉及)
22) 疫苗检测(如涉及)
23) 生物制品及先进治疗药物检测(如涉及)
3、初步筛选
4、现场检查
5、报告与整改
6、列名决定
7、持续监督
一旦被列入名单,实验室必须维持其合规状态并接受WHO的持续监督:
|
监督机制 |
要求 |
|
年度报告 |
每年3月底前提交,涵盖服务摘要、样品分析数据、OOS调查、客户投诉、能力验证结果等。 |
|
变更通知 |
任何可能影响实验室列名状态的重大变更(如设施、关键人员、设备)必须立即通知 WHO。 |
|
重新检查 |
常规至少每3年一次;发生重大变更、收到投诉或能力验证不佳时随时进行。 |
如果您想了解更多GMP解决方案,可以访问www.gempexchina.com/gmp-knowledge获取。在那里,您将更深入了解gempex德恩咨询的GMP服务。
如果您有具体的合规难题,请通过以下方式联系我们。
热线:400 166 2002
邮箱:info-cn@gempex.com
关于gempex德恩咨询
gempex德恩咨询深耕GMP合规领域24年,致力于为全球的生命科学企业提供合规、高效及可执行的GMP解决方案,帮助制药、生物技术、原辅包、医疗器械等各方达到NMPA、EU、FDA、PIC/S等GMP标准,减少合规及药品安全风险。
目前,我们拥有60多位经验丰富的GMP专家,全球累计执行项目超过5000个,累计为1000多个客户提供专业服务,业务遍布20多个国家,并与众多知名药企建立了长期的合作关系。