冗余过滤、双重过滤、除菌过滤、完整性测试

在日常的除菌过滤工艺中,冗余过滤和双重过滤看起来都是两个滤芯串联,它们物理形态相似,但在设计目的、验证方法和日常检测上却有本质区别。不少从业者虽然听说过这两个概念,却未必做过系统性的了解和区分。
如果说上一篇除菌过滤文章关注的是PUPSIT“测不测”的现实困境,那今天这篇要解决的是“怎么配置”的概念混淆。我们结合PDA TR26新修订版指南,通过一篇文章为您讲清冗余和双重。
先搞清楚定义
冗余过滤(Redundant filtration):是指两个过滤器串联安装,前端过滤器起保护作用,用于延长后端主过滤器的使用寿命或应对高负荷挑战。后端除菌级过滤器承担除菌任务。生产后只需对后端主过滤器进行完整性测试。
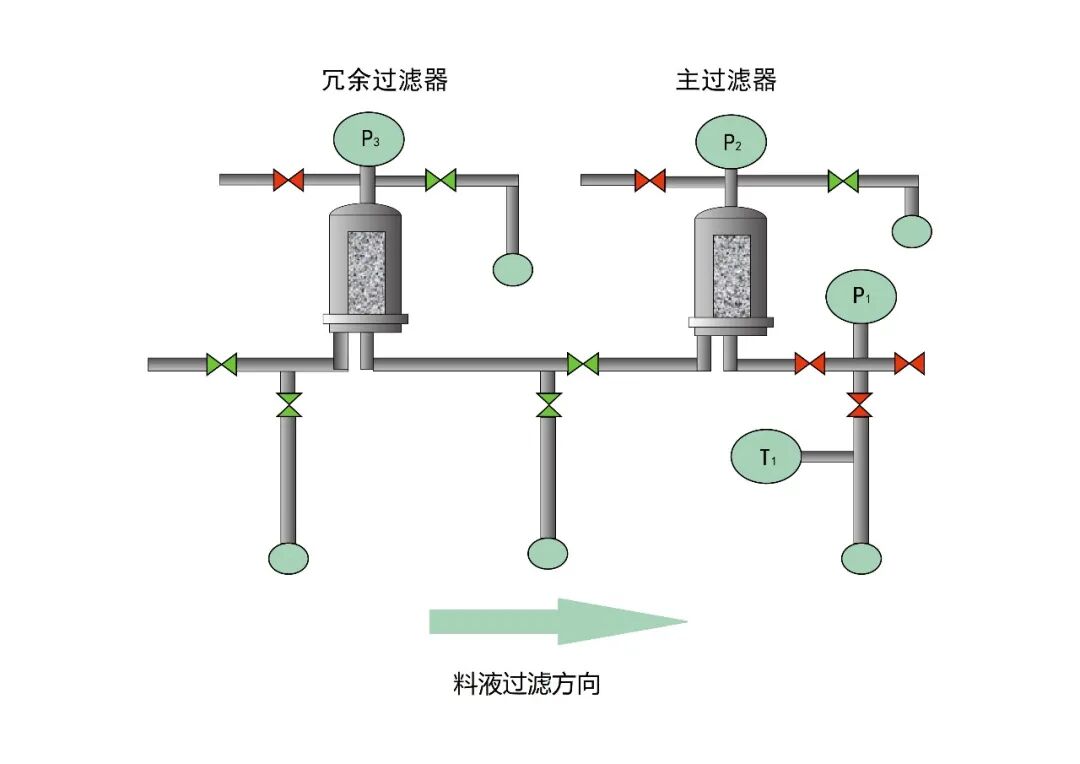
双重过滤(Double filtration / Two- filter sterilization):是指两个除菌级过滤器串联安装,两个过滤器共同承担除菌任务。任何一个滤芯失效,都可能影响整个系统的除菌能力。生产后,应分别对两个过滤器进行完整性测试。
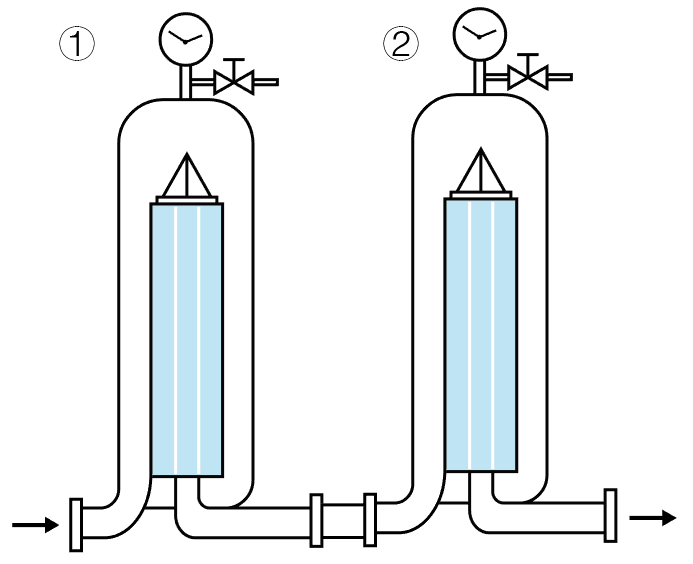
双重过滤图示
常见误区:两个滤芯串联就是冗余过滤吗?
并不是,串联只是物理形态,判断是冗余还是双重,由设计逻辑和验证策略决定。
一张表看懂核心区别
|
对比 |
冗余过滤 |
双重过滤 |
|
除菌关键点 |
依靠单一滤芯的除菌能力 |
依靠两个滤芯作为一个整体完成除菌 |
|
设计逻辑 |
前端保护后端,后端是最后防线 |
两个共同承担除菌任务 |
|
验证逻辑 |
证明“单靠这一个也能截留” |
证明“两个一起工作能截留” |
|
工艺验证(PV)细菌截留试验 |
使用一个滤芯开展试验 |
使用两个滤芯开展试验 |
|
工艺性能确认(PPQ)批次 |
建议采用两个滤芯,以匹配冗余过滤的实际工艺设计与最差条件参数挑战 |
采用两个滤芯,与实际生产配置一致 |
|
使用前灭菌后完整性测试(PUPSIT) |
测试两个过滤器 |
测试两个过滤器 |
|
生产后完整性测试(PUIT) |
仅测试后端主过滤器,前端冗余过滤器不用测 |
分别测试两个过滤器 |
法规依据:PDA TR26、EU GMP Annex 1、中国GMP指南、除菌过滤技术及应用指南2018
关于二者的常见疑问
Q1:为什么冗余过滤验证时用单一滤芯?
冗余过滤的“冗余”体现在:即使前端保护功能失效,后端依然能独立提供完整的除菌保障。验证时用单一滤芯,就是要证明“后端确实有这个能力”。如果用两个滤芯验证,万一前端帮了忙,反而测不出后端的真实水平。
Q2:为什么冗余过滤做3批次,有时用一个滤芯?有时用两个?
对于双重过滤而言,不管是PV还是PPQ,都使用两个滤芯。
Q3:为什么PPQ批次都建议采用两个滤芯?
冗余过滤在PV时用单一滤芯证明除菌能力,但在PPQ批次(即从临床转向商业化生产的过渡批次)时,要用实际生产的配置(两个滤芯)来运行,以验证整个工艺在真实条件下的表现。
Q4:为什么冗余过滤生产前PUPSIT要测两个?生产后PUIT只测一个?
冗余过滤中,两个过滤器都被视为具备独立完成除菌过滤的能力,前端过滤器虽然在事实上过滤了药液,但后端过滤器定义为主过滤器。
PUPSIT是过滤操作前滤芯完整性的直接证明,当生产过程出现主过滤器损坏的情况,除菌过滤的影响评估依赖于前端过滤器完整性。如果不对前端过滤器开展PUPSIT,则无法评估其在过滤操作开始前的完整性——所以做PUPSIT时两个都得查。
分不清会有什么问题?
在日常工作中,如果将二者混为一谈,可能会出现以下问题:
分清两者,才能避免“该测的没测”/“不该测的多测”。
3步快速判断:你的配置是哪种?
看验证报告:细菌截留试验用了几个滤芯?
看SOP:PUIT写的是“测两个滤芯”还是“只测后端”?
看工艺流程图:两个滤芯标注的功能是什么?
希望通过今天的梳理,能够帮助大家在工艺验证执行中,更清晰、更准确地理解和应用这两种过滤配置。如果你觉得有帮助,请转发给更多的人吧!
(本文章为gempex德恩咨询原创。如需转载,请注明来源于gempex德恩咨询。)
gempex德恩咨询作为源自德国的GMP咨询与执行机构,深耕合规领域20余年,专注将复杂法规要求转化为可落地的企业实践。我们的专家团队在工艺验证领域拥有丰富的经验,尤其是无菌工艺验证、清洁验证、分析方法验证等方面具备实战经验。我们可为您提供以下支持:
如果您需要第三方审计或能够落地的合规解决方案,欢迎联系我们。点击下方图片,了解我们完整的合规服务类型。

关注“二维码”,或邮件/电话联系我们
服务热线:400 166 2002
邮箱:info-cn@gempex.com
如果您想了解更多GMP解决方案,可以访问www.gempexchina.com/gmp-knowledge获取。在那里,您将更深入了解gempex德恩咨询的GMP服务。
关于gempex德恩咨询
gempex德恩咨询深耕GMP合规领域24年,致力于为全球的生命科学企业提供合规、高效及可执行的GMP解决方案,帮助制药、生物技术、原辅包、医疗器械等各方达到NMPA、EU、FDA、PIC/S等GMP标准,减少合规及药品安全风险。
目前,我们拥有60多位经验丰富的GMP专家,全球累计执行项目超过5000个,累计为1000多个客户提供专业服务,业务遍布20多个国家,并与众多知名药企建立了长期的合作关系。