2025-07-14
2025年7月11-12日,第六届生物药质量科学大会(QbD2025)在北京朝阳万达文华酒店圆满举办。本届大会以"质取工艺、设计未来"为主题,汇聚全国生物药领域专家、企业代表及监管机构,共同探讨前沿技术、政策法规与创新药出海战略。
作为深耕GMP合规23年的国际化服务商,gempex德恩咨询受邀参与此次盛会,通过主题演讲、展位互动及专家咨询等形式,全面展示其在全球化合规领域的专业实力。

主题演讲:直击全球化合规核心挑战
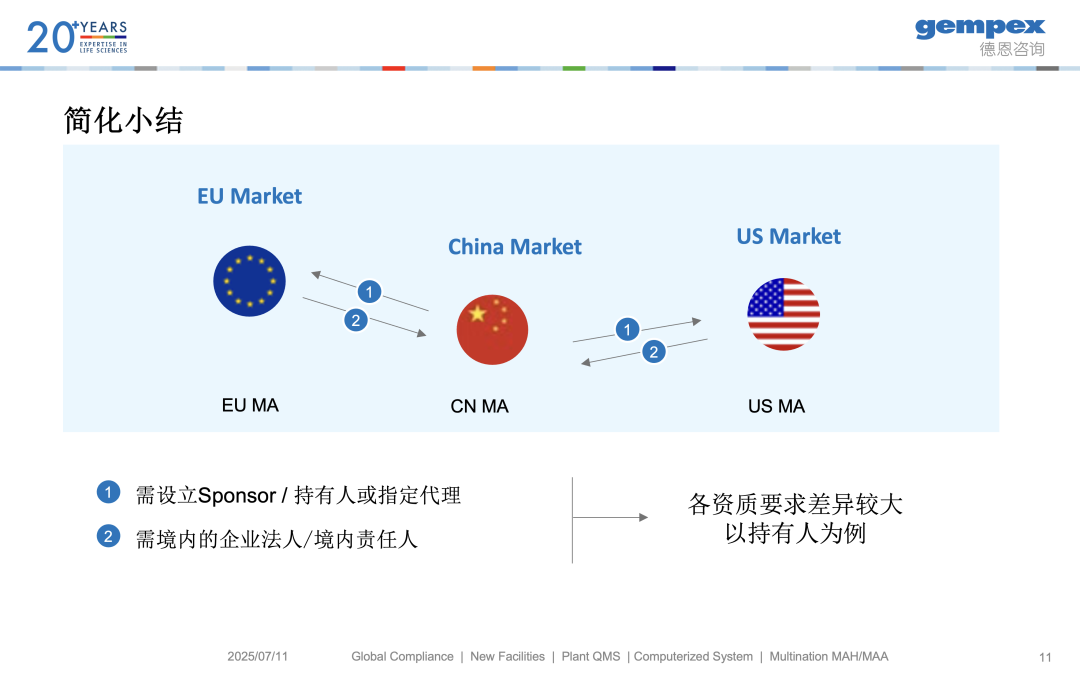
7月11日下午,gempex德恩咨询中国区副总经理及资深GMP专家冯翠容女士在"生物类似药与创新药全球化路径"分论坛发表题为《全球化路径的持有及准入制度与质量体系管理要求》的主题演讲,结合政策解读与实战案例,为生物药企业布局全球 化提供清晰的合规路径。

核心内容 / CONTENT