#EMA #3DP #制药三维打印 #增材制造 #固体制剂 #质量要求 #GMP要求 #药墨 #gempex德恩咨询

EMA于2026年3月12日发布了一份问答(Q&A)文件《口服固体制剂3DP技术(增材制造技术)实施问答》,为 3DP技术在固体口服制剂生产中的应用,提供了具体的合规指导。
要理解这份文件,首先需要了解3DP技术在制药中的基本原理与特点。
在制药行业中,什么是3DP技术?
3DP:Three-Dimensional Printing,即三维打印,也叫增材制造。在制药中,它通过逐层打印“制药墨水”来制造固体药片、含片等制剂。
制药墨水(Pharma Ink,以下简称“药墨”):药物研发关键中间体,指装载在卡式瓶(cartridge)/针筒(syringe)中的制剂,含原料药、辅料等混合物。
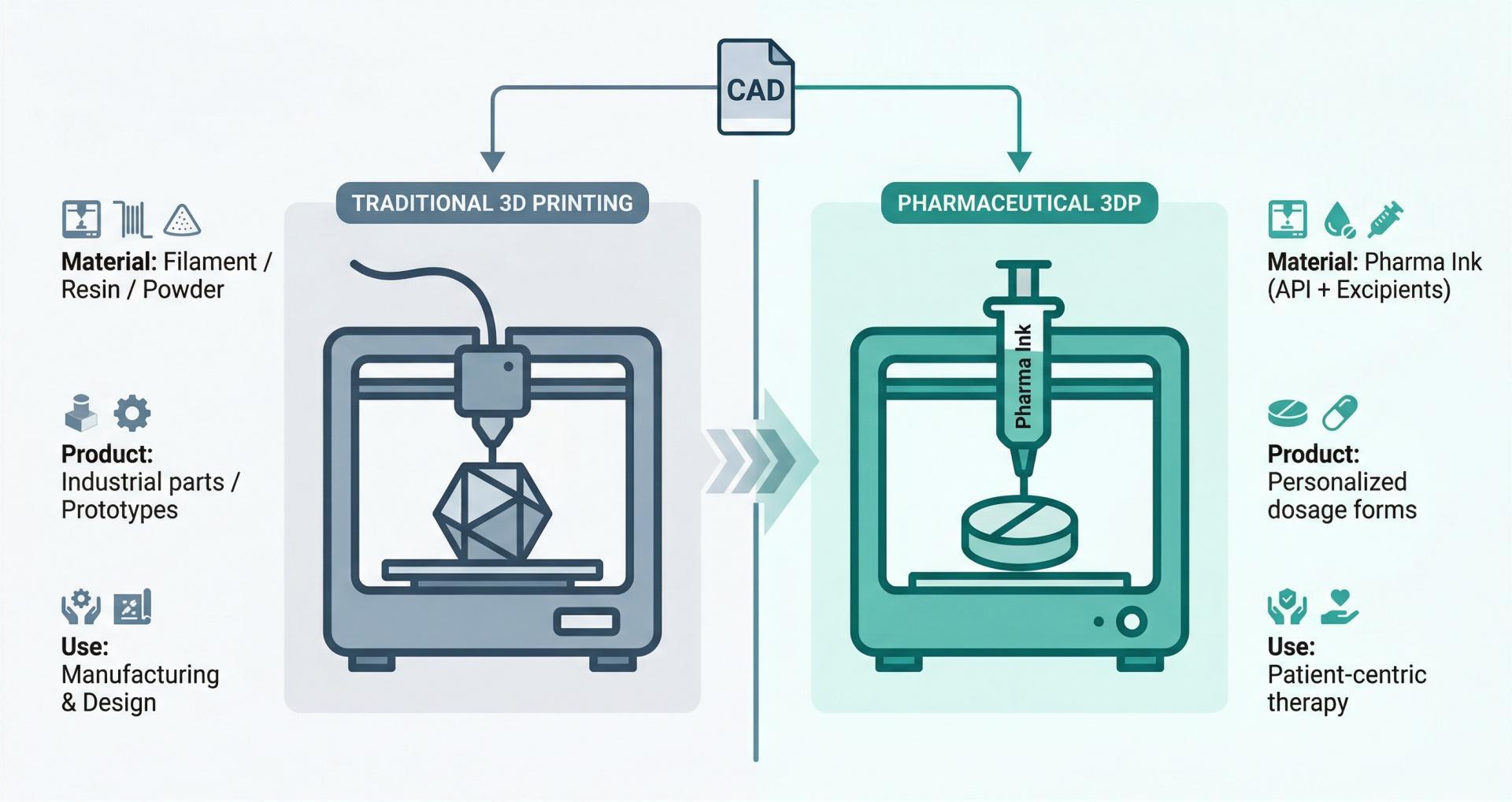
与传统3D打印对比:传统3D打印多用金属、树脂等材料制造非生物制品;制药3DP使用含活性成分的“药墨”,产品需满足含量均匀度、溶出度等药品专属质量要求。
与传统压片对比:传统压片依赖模具大批量生产,换批慢;3DP可以实现快速制造,配备紧凑设备,生产步骤更少,采用自动化和数字化的生产流程,并具备更快的换型能力,可灵活调整剂量和形状,适合小批量、个性化用药,但增加了药墨稳定性、清洁验证等新挑战。
从技术原理到合规指导
了解了技术原理之后,一个关键问题随之而来:这项技术如何满足药品生产的质量和GMP要求?
以下从质量要求和GMP要求两方面进行梳理:
1.药品生产中应用3DP的质量要求
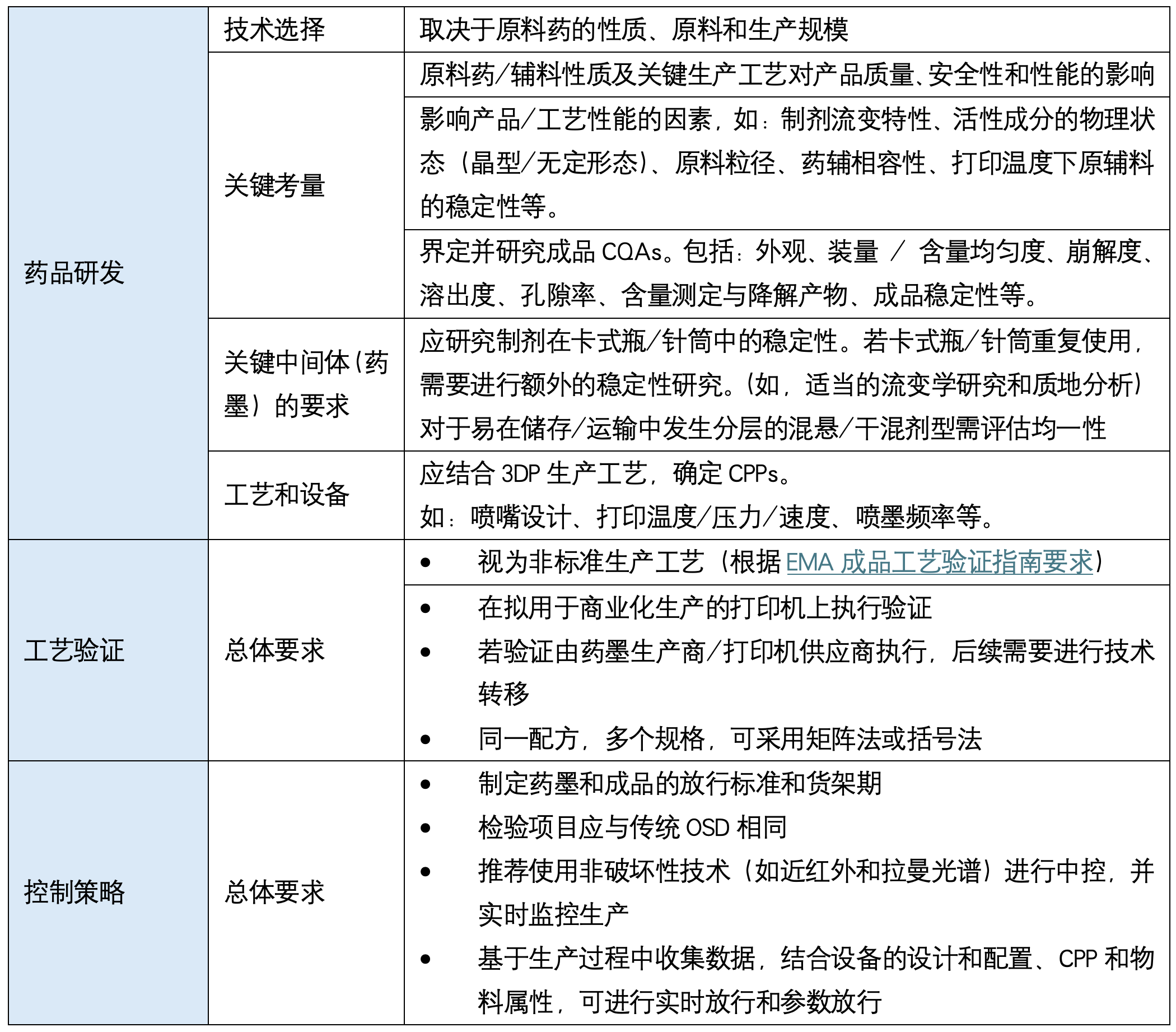
(点击图片放大查看)
2. 药品生产中应用3DP的GMP要求
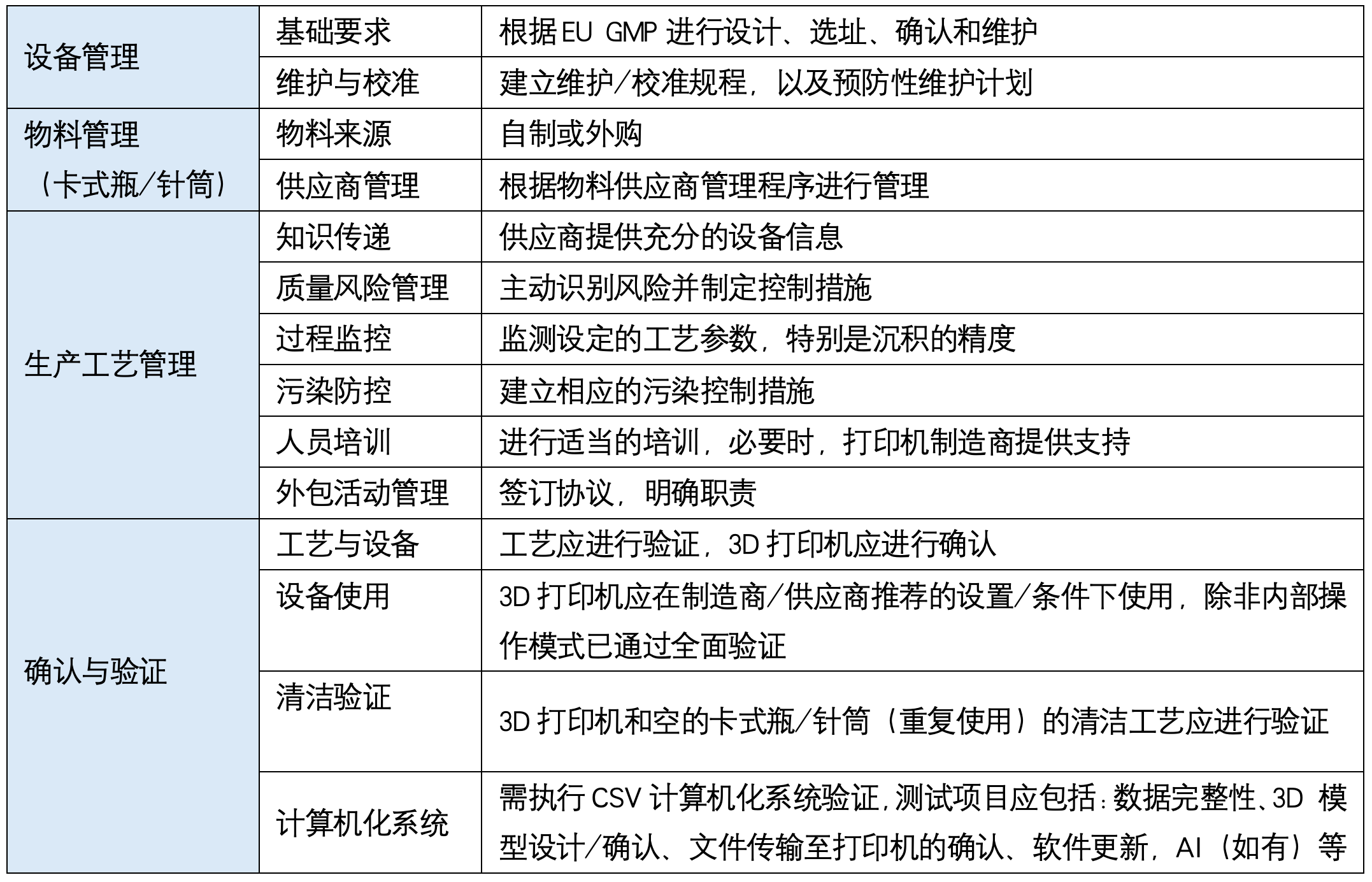
(点击图片放大查看)
总结
综合EMA本次Q&A,3DP固体制剂的合规关注点主要集中在:
3DP技术虽然新兴,但仍处于现有GMP合规框架之内。gempex德恩咨询作为源自德国的GMP咨询与执行机构,深耕GMP合规领域20余年,我们的专家团队拥有丰富的经验,可为您提供以下支持:
如果您的产品需要能够落地的合规解决方案,欢迎联系我们。
服务热线:400 166 2002
邮箱:info-cn@gempex.com

点击下方图片,了解我们完整的合规服务类型。让我们用专业的合规能力,为您的产品质量保驾护航。

如果您想了解更多GMP解决方案,可以访问www.gempexchina.com/gmp-knowledge获取。在那里,您将更深入了解gempex德恩咨询的GMP服务。
关于gempex德恩咨询
gempex德恩咨询深耕GMP合规领域24年,致力于为全球的生命科学企业提供合规、高效及可执行的GMP解决方案,帮助制药、生物技术、原辅包、医疗器械等各方达到NMPA、EU、FDA、PIC/S等GMP标准,减少合规及药品安全风险。
目前,我们拥有60多位经验丰富的GMP专家,全球累计执行项目超过5000个,累计为1000多个客户提供专业服务,业务遍布20多个国家,并与众多知名药企建立了长期的合作关系。